Фтор
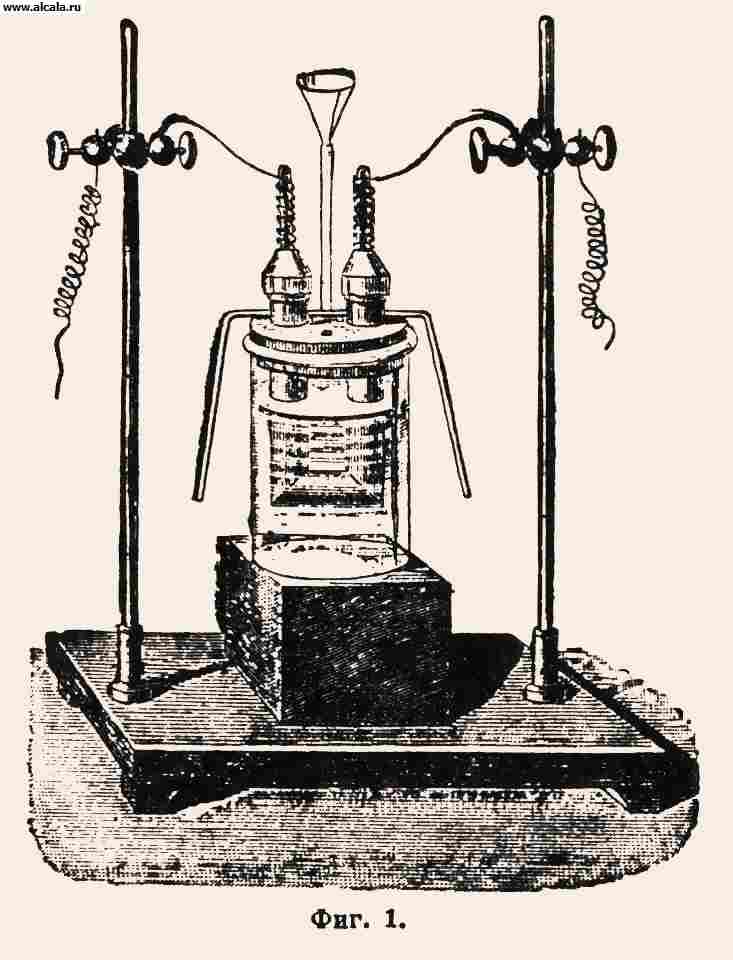
Фтор (хим. обозначение F, частица F 2, атомный вес — 19,05). Фтор — химический элемент, составляющий вместе с хлором, бромом и йодом одну особую характерную группу тел, так называемую группу галоидов. Свое название Фтор получил от греческого слова φτοριος — разрушающий, благодаря способности соединения Фтор с водородом — фтористого водорода или плавиковой кислоты НF — разъедать стекло. Фтор довольно значительно распространен в природе, хотя далеко не так, как хлор. Здесь прежде всего можно назвать плавиковый шпат — CaF 2, затем криолит — двойная соль фтористых натрия и алюминия AlF 3 3NaF, встречающаяся в больших массах, в особенности в Гренландии; в малых долях Фтор входит в состав многих минералов, например апатита и вообще фосфоритов, амблагонита, топаза, лепидолита, амфибола, амианта и проч., его находят во многих растениях, в костях животных, в крови, в речной воде и проч. Соединения Фтор стали известными в средние века. О плавиковом шпате упоминает еще Basilius Valentinus в конце XV столетия, как о веществе, которое прибавляется к руде для облегчения плавкости, о способности плавикового шпата светиться при нагревании пишет Eisholz в 1677 г. Нюрнбергский мастер Швангардт в 1670 г. нашел, что плавиковый шпат с серной кислотой разъедает стекло. Это явление было подробнее изучено сто лет спустя Марграфом (в 1768 г.) и, главным образом, Шееле в 1771— 8 1 гг., который показал, что в этих условиях получается особая кислота; для хранения ее он применял свинцовые сосуды. Полученная Шееле плавиковая кислота содержала воду. Гей-Люссак и Тенар в 1808—09 гг. произвели подробные исследования для получения безводной плавиковой кислоты; хотя кислота получилась достаточно чистая, но далеко не безводная; ими же был открыт газообразный фтористый бор. Сообразно с господствовавшими воззрениями, что в состав кислот должен входить кислород, плавиковая кислота рассматривалась как содержащая кислород, пока в 1810 г. Ампер не указал на сходство ее с соляной кислотой и, по аналогии с последней, определил ее как соединение водорода с неизвестным еще элементом, названным им Ф. Дж. Дэви исследовал фтористый бор и кремний в 1812 г., а Берцелиус — фтористые металлы. Получить Фтор в свободном состоянии и изучить его физические и химические свойства, несмотря на все усилия, удалось только в 1886 г. Муассану; все затруднение состояло в чрезвычайно энергичной способности Фтор соединяться с многочисленными телами. История попыток получения Фтор составляет одну из замечательных страниц истории развития неорганической химии. Первые наиболее серьезные исследования в этом направлении были произведены Гумфри Дэви, который разделял воззрения Ампера на состав плавиковой кислоты; он прежде всего поставил опыт, чтобы убедиться в том, что плавиковая кислота не содержит кислорода. С этою целью он приготовил ее аммиачную соль (фтористый аммоний NH 4 F) и подверг ее сильному прокаливанию в платиновом приборе. Соль только сублимировалась без образования следов воды, что должно было бы произойти, если бы в состав ее входил кислород. Дэви для выделения Фтор произвел ряд работ, которые велись двумя методами: 1) он применил электролиз и 2) действием высокой температуры на фтористые соединения. Электролизу подвергались плавиковая кислота и фтористые металлы в приборах из платины или сплавленного хлористого серебра при помощи очень сильной батареи. При электролизе плавиковой кислоты ток шел пока кислота содержала воду, а затем постепенно падал, и Фтор не получался; кислота, несмотря на охлаждение, обращалась в пар, который наполнял лабораторию и делал пребывание в ней невозможным. Дэви был очень болен после этих опытов, так же как и Гей-Люссак и Тенар, которые работали с плавиковой кислотой. Безуспешно было и пропускание электрических искр в плавиковую кислоту. Дэви затем подвергал действию хлора фтористые соединения калия, натрия, ртути, серебра в приборах из различных материалов (стекла, платины, золота, угля, серы и проч.) и при различной температуре. При всех попытках результат получался неудовлетворительный, так как выделившийся Фтор тотчас соединялся с материалом прибора. Заканчивая изложение своих попыток получить Ф., Дэви высказал мысль, что результаты, может быть, были бы более удачны, если бы применялись приборы из плавикового шпата. После Дэви Aim é (1833) разлагал хлором фтористое серебро в стеклянном приборе, покрытом тонким слоем каучука; в результате каучук был обуглен, а фтор не получен. Вслед за тем члены ирландской академии, братья Knox, делали попытки разложить хлором фтористое серебро в приборе из плавикового шпата. Попытка оказалась безуспешной, с одной стороны, как показал потом Фреми, потому, что хлор стремится скорее дать продукты присоединения, чем вытеснить Ф., а с другой — кроме того, благодаря тому обстоятельству, что очень трудно получить вполне безводное фтористое серебро и фтористую ртуть. Подобный же результат получился и в работе Луйе (1876) с действием хлора или йода на фтористую ртуть в таком же приборе. Братья Knox, подобно Дэви, сильно пострадали от вредного действия паров HF, и один из них должен был прожить 3 года в Неаполе, чтобы сколько-нибудь поправить свое здоровье; Луйе же, который не принимал достаточных предосторожностей, поплатился своей жизнью. Около 1850 г. предпринял работу над Ф. Фреми. Он приготовил совершенно безводную фтористо-водородную кислоту, указал на существование многочисленных соединений фтористых металлов с фтористо-водородной кислотой и изучил действие на них кислорода и хлора при высокой температуре в платиновых приборах. Для опытов служили фтористые свинец, сурьма, ртуть и серебро. Найдя, что, несмотря на все усилия, он не может получить эти вещества безводными, Фреми обратился к плавиковому шпату, который часто встречается в природе в чистом виде и совершенно безводный. Плавиковый шпат плавился при высокой температуре в платиновых сосудах и подвергался электролизу; на положительном электроде — платиновом стержне — выделялись пузырьки газа, который быстро разъедал электрод. Этот газ выделял йод из его соединений; но опыт быстро прекращался, так как получающийся на отрицательном полюсе металлический кальций скоро продырявливал платиновый сосуд, и все нужно было начинать вновь, что стоило больших денег и требовало много времени. После Фреми изучал электролиз фтористо-водородной кислоты Гор; он нашел, что безводная кислота, приготовленная по способу Фреми, не проводит тока, на что указывал еще Фарадей; если она содержит воду, то электролиз идет за счет этой последней; при электролизе же расплавленных фтористых металлов, например фтористого серебра или кислого фтористого калия KF.HF, анод быстро разъедался, но никакого газа не получалось. Каммерер действовал йодом при 60° на фтористое серебро в запаянной стеклянной трубке, из которой был вытеснен воздух парами йода; он получил газ, не разъедающий стекло, и принял его за Ф., но Пфаундлер показал, что это была смесь фтористого кремния SiF 4 с кислородом. Также неудачны были попытки Бодримона и др. В таком положении находился вопрос о получении Ф., когда приступил к нему Муассан. При начале своих исследований он держался той руководящей идеи, что если Фтор аналогичен галоидам, то для получения его следует скорее обратиться к его соединениям с металлоидами (кремнием, фосфором, мышьяком) или к фтористому водороду, чем к металлическим производным, так как, например, хлор легче получить из хлористого фосфора, чем из хлористого кальция, натрия или калия. С другой стороны, так как все предшественники указывали, что Фтор обладает чрезвычайно выраженной способностью к соединениям, то становилось ясным, что выделение Фтор должно производиться при температуре возможно более низкой, чтобы понизить его энергию к соединению. Исходя из этих соображений, Муассан выбрал прежде всего объектом своих исследований фтористый кремний SiF 4; но с первых же шагов он должен был оставить его, так как оказалось, что SiF 4 принадлежит к очень прочным телам и даже щелочные металлы разлагают его только при темно-красном калении. Это и не удивительно, если принять во внимание, как это оказалось потом, что кремний воспламеняется в атмосфере Ф., отделяя, по расчету Гюнца, 134,7 калорий. При пропускании искр в 4 см от спирали Румкорфа SiF 4 оставался без изменения. Фтористый кремний пропускали затем через накаленную губчатую платину, в надежде, что в этих условиях образуется фтористая платина, которая при высокой температуре будет выделять Ф.; при этих опытах получился газ, который разъедал немного стекло; но, вообще говоря, SiF 4 мало изменялся. Подобные же опыты были повторены с фтористыми соединениями фосфора PF 3, PF5, РFO 3, но тоже без успеха. Затем был приготовлен фтористый мышьяк AsF 3, вещество жидкое при обыкновенной температуре и более ядовитое, чем HF, и подвергнут действию тока до 25 элементов Бунзена. Фтористый мышьяк помещался в платиновый тигель, который служил отрицательным электродом, а положительным была платиновая проволока. При этом в жидкости быстро выделялся мышьяк, который садился на стенки тигля, а около проволоки получались пузырьки газа, и проволока разъедалась. Опыт продолжался недолго, так как выделившийся мышьяк по своей малой электропроводности прекращал ток. Чтобы сделать жидкость более проводящей ток, к ней прибавлялась безводная фтористо-водородная кислота и фтористые металлы; наиболее удобным оказался K F.HF; вместо тигля употреблялась также платиновая трубка (вроде пробирки), которая при опыте охлаждалась льдом, и число элементов пришлось довести до 90, чтобы избежать образования слоя мышьяка, который тогда оставался в виде мути. Хотя, при совершенно чистых материалах, и получался на положительном электроде газ, но он быстро поглощался жидкостью, причем образовался, вероятно, AsF 5 и газ почти не выделялся. Думать, что когда большая часть AsF 3 превратится в AsF 5, то результат электролиза будет более ощутителен, едва ли возможно, так как AsF 5, вероятно, стал бы действовать на взмученный в жидкости мышьяк, превращая его вновь в AsF 3. Были сделаны попытки приготовить химическим способом AsF 5, но они оказались бесплодными. Тогда все внимание было обращено на электролиз фтористо-водородной кислоты. Так как при электролизе ее оба продукта разложения должны были получиться в газообразном состоянии, то для разделения их аппарату была придана U-образная форма; он был сделан из платиновой трубки, отверстия которой закрывались парафинированными пробками; через них проходили стержни из иридистой платины, служившие электродами. В каждом колене U-образной платиновой трубки сбоку, под пробками, находились боковые трубочки для выхода газообразных продуктов разложения. Весь прибор был поставлен в стеклянную банку и окружен хлористым метилом СН 3 Cl, кипящим при обыкновенном давлении при —23° (а понижая давление, с ним можно иметь температуру —50°). Так как безводная фтористо-водородная кислота не проводит тока, то к ней был прибавлен кислый фтористый калий KF.HF, который хорошо растворяется в ней. Через прибор был пропущен ток от 50 элементов Бунзена, и хотя разложение происходило легко и на отрицательном полюсе получался водород, но Фтор не было. Когда после часового действия прибор был разобран, то оказалось, что пробка, покрытая парафином, у положительного полюса была обуглена на 1 см выделившимся Ф., и сильно разъеден положительный электрод и платиновая трубка над поверхностью жидкости. Оставалось сделать пробки из материала, на который Фтор не действует, и вопрос о получении Фтор был решен. Пробки были сделаны из плавикового шпата. После многих попыток укрепить их герметически в U-образной трубке (мастики разъедались Ф.) Муассан остановился на том, что снабдил их нарезками и ввинчивал в трубку; сверху же покрывал мастикой, которая тогда стало гораздо меньше страдать от действия Фтор (фиг. 1).
Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона. — С.-Пб. Брокгауз-Ефрон.
Читайте также :
Фторангидриды кислотФторангидриды кислот R.CO.F — получаются обменным разложением, аналогично фторопроизводным (см.) жирных углеводородов, из соответствующих хлорангидридов при действии на них AgF, AsF 3, SbF3,...
Фторопроизводные углеводородовФторопроизводные углеводородов — Из Ф. жирных углеводородов первым был получен (Дюма и Пелиго, 1835) фтористый метил СH 3 F при нагревании метилсернокалиевой соли K(CH 3)SO4 с фтористым кали...
Фуа, графский родФуа, графский род (Foix) — графский род в южной Франции, ведет свое происхождение от графа Рожера I из Каркасона († в 1012 г.). Более известны: 1) граф Раймонд Рожер, наследовал своему отц...
Энциклопедии и словари на ALCALA.RU 2005-2011 год. - Значение слова в Бесплатных онлайн словарях - справочниках
Все тексты выложены на сайте для не коммерческого использования и взяты из открытых источников.
При использовании материалов сайта активная ссылка на ALCALA.RU обязательна!!
Все права на тексты принадлежат только их правообладателям!!